
- Forfatter Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Sist endret 2025-01-22 17:07.
I null - ordrekinetikk , den vurdere av en reaksjon gjør det ikke avhengig av substratkonsentrasjonen. t 1 /2 formel for en nullordensreaksjon foreslår halv - liv avhenger av mengden startkonsentrasjon og hastighetskonstant.
Deretter kan man også spørre seg, hva er halveringstiden for en nullordensreaksjon?
96 sekunder
Dessuten, hvordan finner du halveringstiden til en hastighetskonstant? Strategi:
- Bruk ligning 3 for å beregne halveringstiden til reaksjonen.
- Multipliser startkonsentrasjonen med 1/2 til potensen som tilsvarer antall halveringstider for å oppnå de gjenværende konsentrasjonene etter disse halveringstidene.
- Trekk den gjenværende konsentrasjonen fra den opprinnelige konsentrasjonen.
Angående dette, hvorfor er halveringstiden til en førsteordens reaksjon konstant?
Med andre ord har den innledende konsentrasjonen av reaktanten ingen innflytelse på halv - liv av reaksjon , dvs. den halv - liv er konstant uavhengig av konsentrasjonen av reaktanten.
Avhenger halveringstiden til en nullordensreaksjon av den opprinnelige konsentrasjonen av reaktanten?
Derfor, fra ligningen ovenfor, vi kan konkludere med at halveringstiden for en nullordensreaksjon avhenger på initial konsentrasjon av reagerende arter og hastighetskonstanten, k. Det er direkte proporsjonalt med startkonsentrasjonen av reaktanten mens den er omvendt proporsjonal med hastighetskonstanten, k.
Anbefalt:
Hvordan forholder ordet matrise seg til mitokondrier?
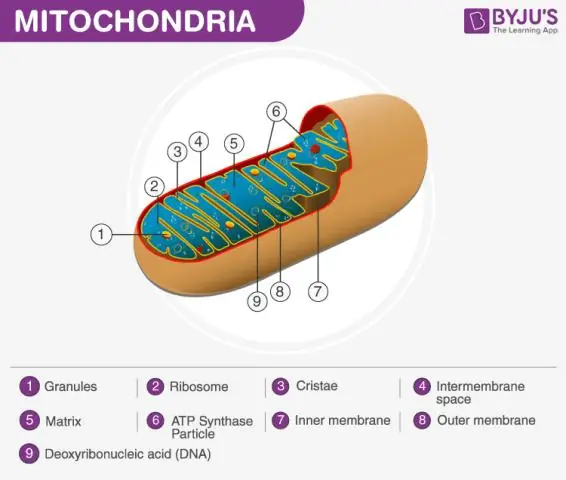
Mitokondriematrisen definert Mitokondriet består av en ytre membran, en indre membran og et gellignende materiale kalt matrisen. Denne matrisen er mer viskøs enn cellens cytoplasma da den inneholder mindre vann. Dette er et viktig trinn i cellulær respirasjon, som produserer energimolekyler kalt ATP
Hvordan forholder svaret ditt fra spørsmål 1 seg til Linnaean klassifiseringssystemet?

Hvordan forholder svaret ditt fra spørsmål 1 seg til Linnaean-klassifiseringssystemet? Mitt svar fra spørsmål 1 relaterer seg til Linnaen-klassifiseringssystemet ved å identifisere det indre og ytre av organismen først. Etter det bruker Linnean-klassifiseringen farge og størrelse for å identifisere organismen
Hvordan forholder den østafrikanske riften seg til platetektonikk?

The East African Rift Valley (EAR) er en utviklende divergerende plategrense i Øst-Afrika. De nubiske og somaliske platene skiller seg også fra den arabiske platen i nord, og skaper dermed et "Y"-formet riflingsystem. Disse platene krysser hverandre i Afar-regionen i Etiopia ved det som er kjent som et "trippelkryss"
Hvordan forholder den kinetiske teorien om materie seg til faste stoffer, væsker og gasser?

Den kinetiske molekylære teorien om materie sier at: Materie består av partikler som er i konstant bevegelse. Alle partikler har energi, men energien varierer avhengig av temperaturen stoffprøven befinner seg i. Dette avgjør igjen om stoffet eksisterer i fast, flytende eller gassform
Hvordan forholder befolkningsveksten per innbygger seg til befolkningsstørrelsen?

Befolkningsvekst er målt i antall individer i en populasjon (N) over tid (t). Per innbygger betyr per individ, og vekstraten per innbygger innebærer antall fødsler og dødsfall i en befolkning. Den logistiske vekstligningen antar at K og r ikke endres over tid i en populasjon
