
- Forfatter Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Sist endret 2025-01-22 17:06.
Avogadros lov viser at det er en direkte sammenheng mellom antall mol av en gass og dens volum . Dette kan også vises ved hjelp av ligningen: V1/n1 = V2/n2. Hvis antall mol dobles, vil volum vil doble seg.
På denne måten, hva er formelen for Avogadros lov?
Avogadros lovformel Der "V" er volumet av gassen, "n" er mengden av gassen (antall mol av gassen) og "k" er en konstant for et gitt trykk og temperatur. Faktisk, Avogadros lov , hypotesen satt av ham, var blant de lover hvorpå den ideelle gassen Lov er basert.
I tillegg, hva er et eksempel på Avogadros lov? Avogadros lov sier at volumet av en gass er direkte proporsjonal med antall mol gass. Her er det noe eksempler . Når du sprenger en basketball, tvinger du flere gassmolekyler inn i den. Jo flere molekyler, jo større volum. Begge ballongene inneholder like mange molekyler.
Dessuten, hva sier Avogadros lov, beviser dette laboratoriet loven. Hvordan vet du det?
Et moderne utsagn er : Avogadros lov sier at "like volumer av alle gasser, ved samme temperatur og trykk, har samme antall molekyler." For en gitt masse av en ideell gass , volumet og mengden (mol) av gassen er direkte proporsjonal hvis temperatur og trykk er konstant.
Hvordan forklares loven om å kombinere volumer av Avogadros hypotese?
(en) Loven om å kombinere volumer av Avogadros hypotese : Alle gasser som inneholder like volumer ved samme ytre forhold for temperatur og trykk vil ha like mange molekyler. Disse gassmolekylene reagerer i forholdet små hele tall, så deres (gass) volumer vil også være i forhold til små hele tall.
Anbefalt:
Hvordan finner du imaginære røtter ved å bruke Descartes tegnregel?

Descartes sin tegnregel sier at antallet positive røtter er lik endringer i fortegn til f(x), eller er mindre enn det med et partall (så du fortsetter å trekke fra 2 til du får enten 1 eller 0). Derfor kan den forrige f(x) ha 2 eller 0 positive røtter. Negative reelle røtter
Hvordan finner du den omtrentlige prosentandelen ved å bruke den empiriske regelen?

Finne arealet under kurven fra x = 9 til x = 13. Den empiriske regelen eller 68-95-99,7 %-regelen gir den omtrentlige prosentandelen av data som faller innenfor ett standardavvik (68 %), to standardavvik (95 %) , og tre standardavvik (99,7 %) av gjennomsnittet
Hvordan løser du Avogadros lov?

Ved konstant trykk og temperatur kan Avogadros lov uttrykkes med følgende formel: V ∝ n. V/n = k. V1/n1 = V2/n2 (= k, i henhold til Avogadros lov). PV = nRT. V/n = (RT)/P. V/n = k. k = (RT)/P. En mol heliumgass fyller opp en tom ballong til et volum på 1,5 liter
Hvordan demonstrerer du Avogadros lov?

Avogadros lov er bevis når du sprenger en ballong. Volumet av ballongen øker når du tilsetter mol gass til ballongen ved å blåse den opp. Hvis beholderen som inneholder gassen er stiv i stedet for fleksibel, kan trykk erstattes med volum i Avogadros lov
Hvordan finner du gjennomsnittet ved å bruke Excel?
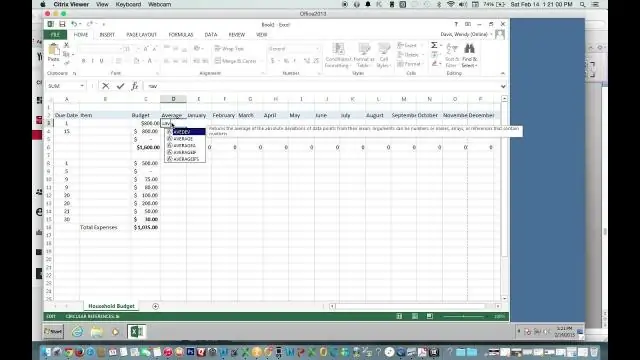
Bruk Autosum for raskt å finne gjennomsnittet Klikk på en celle under kolonnen eller til høyre for raden med tallene du vil finne gjennomsnittet for. På HJEM-fanen klikker du på pilen ved siden av Autosum > Gjennomsnitt, og trykker deretter på Enter
