
- Forfatter Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Sist endret 2025-01-22 17:07.
De ioniseringsenergi av et atom er energi forskjellen mellom elektronet bundet i atomet og elektronet en uendelig avstand fra atomet. Coulombs lov gir det elektriske potensiell energi mellom to punktladninger med avstanden r mellom dem. De energi er omvendt proporsjonal med denne avstanden.
Med tanke på dette, hvordan er ioniseringsenergi relatert til potensiell energi?
Ioniseringsenergier av atomene. For å fjerne et elektron fra et atom, må vi heve potensiell energi fra dens negative verdi til null. I følge Coulombs lov forventer vi at elektroner nærmere kjernen har en lavere potensiell energi og dermed kreve mer energi å fjerne fra atomet.
Deretter er spørsmålet hvorfor øker ioniseringsenergien drastisk? Suksessiv ioniseringsenergiene øker i størrelsesorden fordi antallet elektroner, som forårsaker frastøting, stadig synker. Så mengden av energi nødvendig for å fjerne elektroner utover valenselektronene er betydelig større enn energi av kjemiske reaksjoner og bindinger.
Følgelig, hvordan forholder Coulombs lov seg til elektronegativitet?
I følge Coulombs lov , ettersom atomnummeret øker innenfor en serie atomer, kjernefysisk tiltrekning for elektroner vil øker også, og trekker dermed elektronet(e) nærmere kjernen. Den coulombiske tiltrekningen av kjernen til et atom for elektronene er referert til som elektronegativitet av atomet.
Hva er atomioniseringsenergi?
Den første eller initialen ioniseringsenergi eller EJeg av en atom eller molekylet er energi nødvendig for å fjerne ett mol elektroner fra ett mol isolert gass atomer eller ioner. Du tenker kanskje på ioniseringsenergi som et mål på vanskeligheten med å fjerne elektron eller styrken som et elektron er bundet til.
Anbefalt:
Hvordan forholder ordet matrise seg til mitokondrier?
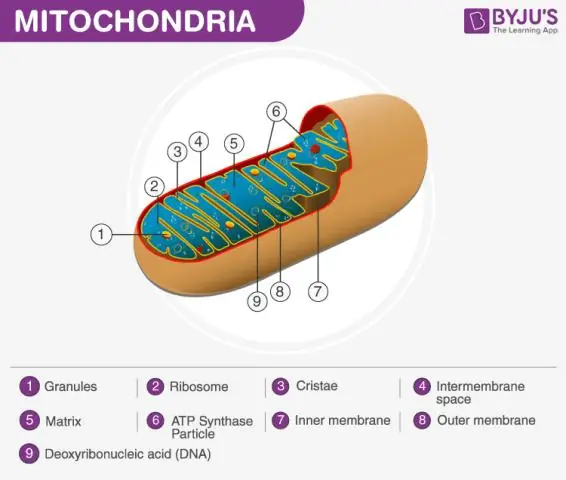
Mitokondriematrisen definert Mitokondriet består av en ytre membran, en indre membran og et gellignende materiale kalt matrisen. Denne matrisen er mer viskøs enn cellens cytoplasma da den inneholder mindre vann. Dette er et viktig trinn i cellulær respirasjon, som produserer energimolekyler kalt ATP
Hvordan forholder svaret ditt fra spørsmål 1 seg til Linnaean klassifiseringssystemet?

Hvordan forholder svaret ditt fra spørsmål 1 seg til Linnaean-klassifiseringssystemet? Mitt svar fra spørsmål 1 relaterer seg til Linnaen-klassifiseringssystemet ved å identifisere det indre og ytre av organismen først. Etter det bruker Linnean-klassifiseringen farge og størrelse for å identifisere organismen
Hvordan forholder den østafrikanske riften seg til platetektonikk?

The East African Rift Valley (EAR) er en utviklende divergerende plategrense i Øst-Afrika. De nubiske og somaliske platene skiller seg også fra den arabiske platen i nord, og skaper dermed et "Y"-formet riflingsystem. Disse platene krysser hverandre i Afar-regionen i Etiopia ved det som er kjent som et "trippelkryss"
Hvordan forholder den kinetiske teorien om materie seg til faste stoffer, væsker og gasser?

Den kinetiske molekylære teorien om materie sier at: Materie består av partikler som er i konstant bevegelse. Alle partikler har energi, men energien varierer avhengig av temperaturen stoffprøven befinner seg i. Dette avgjør igjen om stoffet eksisterer i fast, flytende eller gassform
Hvordan forholder halveringstiden til nullordensreaksjonen seg til hastighetskonstanten?

I nullordens kinetikk avhenger ikke reaksjonshastigheten av substratkonsentrasjonen. t 1 /2-formelen for en nullordensreaksjon antyder at halveringstiden avhenger av mengden initialkonsentrasjon og hastighetskonstanten
