
- Forfatter Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Sist endret 2025-01-22 17:07.
Generelt, faste stoffer er tettere enn væsker, som er tettere enn gasser.. Partiklene i det faste berører veldig lite mellomrom mellom dem. Partiklene i en væske vanligvis fortsatt berører, men der er noen mellomrom mellom dem. De gass partikler har store avstander mellom dem.
Folk spør også, har faste partikler mellomrom mellom seg?
De partikler i en fast holdes sterkt sammen. De mellomrom mellom de partikler er veldig små. EN har en fast form og et fast volum fordi partikler kan bevege seg bare litt. De partikler vibrerer frem og tilbake, men forblir i sine faste posisjoner.
Dessuten, hvorfor er faste partikler tett sammen? Partikler ER AVHOLDT VELDIG TETT SAMMEN De holdes tett sammen av sterke tiltrekningskrefter. De holdes i faste posisjoner, men de vibrerer. Fordi det partikler ikke beveg deg, faste stoffer har en bestemt form og volum, og kan ikke flyte.
Bare så, hva er i rommet mellom partiklene?
Fordi det partikler beveger seg, vil en gass fylle enhver beholder den settes inn i. For det er det mellomrom mellom partiklene , kan de presses til et mindre volum når gassen komprimeres.
Hvor adskilt er partiklene i hver materietilstand?
Partikler i en: gass er bra separert uten vanlig ordning. væske er tett sammen uten regelmessig arrangement. solide er tettpakket, vanligvis i et vanlig mønster.
Anbefalt:
Hva er de 3 typene krystallinske faste stoffer?

Krystallinske faste stoffer består av repeterende, tredimensjonale mønstre eller gitter av molekyler, ioner eller atomer. Disse partiklene har en tendens til å maksimere plassene de opptar, og skaper solide, nesten ukomprimerbare strukturer. Det er tre hovedtyper av krystallinske faste stoffer: molekylære, ioniske og atomære
Kan faste stoffer ha en pH?
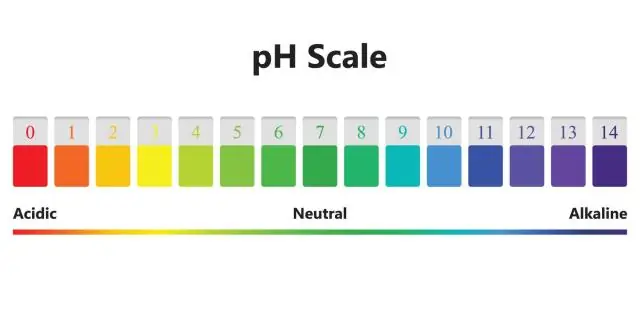
I den faste fasen er det imidlertid ikke noe som heter løsning. Per definisjon er pH relatert til konsentrasjonen av hydrogenionet solvatisert i løsning. Det kan være en vandig løsning, hvor pH-verdien typisk kan variere fra ca. -2 til ca. 16
Hva er forskjellen mellom molekylære faste stoffer og kovalente faste stoffer?

Molekylære faste stoffer - Laget av atomer eller molekyler holdt sammen av London-spredningskrefter, dipol-dipolkrefter eller hydrogenbindinger. Et eksempel på en molekylær solidis sukrose. Kovalent-nettverk (også kalt atomiske) faste stoffer – Laget av atomer forbundet med kovalente bindinger; de intermolekylære kreftene er også kovalente bindinger
Er partikler faste?

I et fast stoff er disse partiklene pakket tett sammen og kan ikke bevege seg fritt i stoffet. Molekylær bevegelse for partiklene i asolid er begrenset til svært små vibrasjoner av atomene rundt deres faste posisjoner; derfor har faste stoffer en fast form som er vanskelig å endre
Hvilken farge har faste stoffer i det periodiske systemet?

I den periodiske tabellen ovenfor indikerer svarte firkanter elementer som er faste stoffer ved romtemperatur (ca. 22ºC)*, de i blå firkanter er væsker ved romtemperatur, og de i røde firkanter er gasser ved romtemperatur
