Innholdsfortegnelse:
- Forfatter Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Sist endret 2025-01-22 17:06.
For bor vil denne ligningen se slik ut:
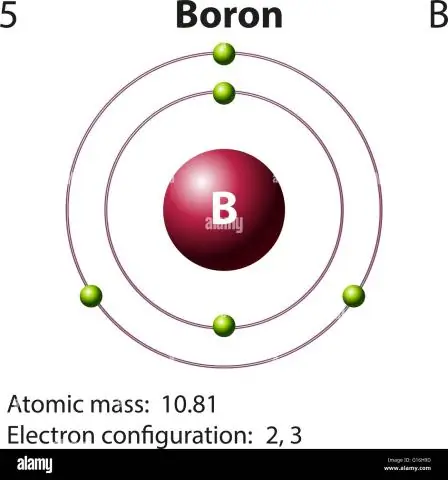
- 5 protoner + 5 nøytroner = 10 atommasse enheter (AMU) eller, for de mer vanlig forekommende bor isotop (ca.
- 5 protoner + 6 nøytroner = 11 AMU.
Når man tar dette i betraktning, hva er atommassen til bor?
10.811 u
Dessuten, hvordan beregner du atommassen til neon? 20.1797 u
Folk spør også, hvordan beregner du atommasse?
Til beregne atommassen av en singel atom av et element, legger du sammen masse av protoner og nøytroner. Eksempel: Finn atommasse av en isotop av karbon som har 7 nøytroner. Du kan se fra det periodiske systemet at karbon har en atomisk antall 6, som er antallet protoner.
Hva har en masse på 1 amu?
En atommasseenhet (symbolisert AMU eller amu) er definert som nøyaktig 1/12 massen til et karbon-12-atom. Karbon-12 (C-12) atomet har seks protoner og seks nøytroner i sin kjerne. I upresise termer er en AMU gjennomsnittet av proton hvilemasse og nøytron hvilemasse.
Anbefalt:
Hvordan beregner du energien til en elektromagnetisk bølge?

Energien som bæres av en bølge er proporsjonal med dens amplitude i kvadrat. For elektromagnetiske bølger betyr dette at intensiteten kan uttrykkes som Iave=cϵ0E202 I ave = c ϵ 0 E 0 2 2, hvor Iave er gjennomsnittlig intensitet i W/m2, og E0 er den maksimale elektriske feltstyrken til en kontinuerlig sinusformet bølge
Hvordan beregner du vekt og balanse til et fly?

Legg til alle øyeblikkene for å finne det totale øyeblikket. Del det totale momentet med bruttovekten for å finne tyngdepunktet. Finn totalvekten og tyngdepunktet på diagrammet for tyngdepunktgrenser i flyets POH for å finne ut om flyet er innenfor tillatte grenser
Hvordan beregner du den gjennomsnittlige atommassen til strontium?

Så vi beregner det ved å ta den vektede massen til hver av isotopene og legge dem sammen. Så for den første massen vil vi multiplisere 0,50% av 84 (amu - atommasseenheter) = 0,042 amu, og legge det til 9,9% av 86 amu = 8,51 amu, og så videre
Hvordan beregner du vekten til en ball?

Et øyeblikk For å bestemme volumet til en kule, må du ta diameteren i potensen 3 og multiplisere den til Pi i tillegg til 1/6. Vekten til en gjenstand beregnes ved å multiplisere volumet med materialets tetthet
Hvordan beregner du omkretsen til et gjerde?

Du kan finne omkretsen til en hvilken som helst form ved å legge sammen lengdene på hver side. Prøv det! Skriv inn lengden på hver side og legg dem til for å finne omkretsen. Mike og onkelen hans trenger fortsatt din hjelp til å finne omkretsen av gården for å vite hvor mye gjerde de skal kjøpe
