
- Forfatter Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Sist endret 2025-01-22 17:07.
Som fortynnet svovelsyre er ideell for redoks titrering fordi det verken er et oksidasjonsmiddel eller et reduksjonsmiddel. HCL, som er en sterk elektrolytt, dissosieres i vann og gir H+ og Cl-ioner. Derav en viss mengde KMnO4 er brukt opp i oksiderende Cl- til Cl2. Side ved side KMnO4 oksiderer oksalation til CO2.
Folk spør også hvorfor h2so4 brukes til titrering av KMnO4?
Svovelsyre tilsettes for å forhindre hydrolyse og for å gi overskudd av H+ ioner i løsningen for å fortsette reaksjonen og også svovelsyre er stabil mot oksidasjon. Fra reaksjonen ovenfor er det tydelig at det kreves 8 mol H+-ioner per mol MnO4- so svovelsyre gir det nødvendige hydrogenionet.
Vet også hvorfor KMnO4 brukes i titrering? Og dermed KMnO4 fungerer som sin egen indikator. Kaliumpermanganat er et oksidasjonsmiddel, som er av dyp fiolett farge. Når brukt i redoks titrering , blir det redusert til brunfarget Mn2+ ion (i sure medier) ved endepunktet og fargeendring ved endepunktet kan enkelt oppdages.
Angående dette, hvorfor legger vi til Dil h2so4 i titrering?
Svovelsyre ( H2SO4 ) brukes i redoksen titrering prosess fordi den gir H(+)-ionene som er nødvendige for at reaksjonen skal skje raskere mens sulfat(-)-ionene knapt reagerer under reaksjonen. Derfor, svovelsyre tilsettes for å gjøre løsningen sur.
Hvorfor brukes ikke HCl i KMnO4-titrering?
KMnO4 er et veldig sterkt oksidasjonsmiddel og det kan oksidere HCl for å frigjøre klorgass, derfor HCl Kan ikke være brukt å surgjøre kaliumpermanganat løsning i volumetrisk analyse.
Anbefalt:
Hvorfor brukes Ames-testen for mutagener for å teste for kreftfremkallende stoffer MCAT?

Spørsmålet ber eksaminanden forklare hvorfor Ames-testen for mutagener kan brukes til å teste for kreftfremkallende stoffer. I Ames-testen er kjemikaliene som forårsaker mutasjoner i Salmonella-teststammer muligens kreftfremkallende, på grunn av at de muterer DNA og DNA-mutasjoner kan forårsake kreft (B)
Hvorfor Fourier-serier brukes i kommunikasjonsteknikk?

Kommunikasjonsteknikk håndterer hovedsakelig signaler og signaler er derfor av forskjellig type som fortsetter, diskrete, periodiske, ikke-periodiske og mange av mange typer. NåFourier-transformasjon hjelper oss å konvertere tidsdomenesignaler i frekvensdomene. Fordi det lar oss trekke ut frekvenskomponentene til et signal
Hvorfor brukes et konvekst speil som et bakspeil?

Konvekse speil brukes ofte som bakspeil (vingespeil) i kjøretøy fordi de gir et oppreist, virtuelt, forminsket bilde i full størrelse av fjerne objekter med et bredere synsfelt. Konvekse speil gjør det mulig for sjåføren å se mye større område enn det som ville vært mulig med et plan speil
Hvorfor brukes parametriske ligninger?
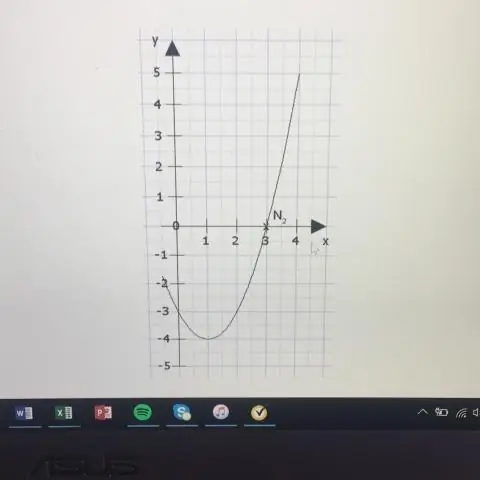
En av fordelene med parametriske ligninger er at de kan brukes til å tegne kurver som ikke er funksjoner, som enhetssirkelen. En annen fordel med parametriske ligninger er at parameteren kan brukes til å representere noe nyttig og derfor gi oss tilleggsinformasjon om grafen
Hva er ligningen som brukes for å beregne den totale mengden energi som brukes av et apparat?

Formelen som forbinder energi og kraft er: Energi = Effekt x Tid. Enheten for energi er joule, kraftenheten er watt, og tidsenheten er den andre
